- Время работы:
- Пн-Вс: 09:00-18:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Главная
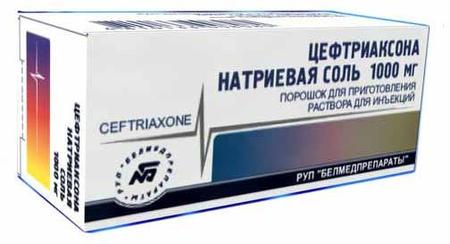
- Ceftriaxone
- Цефтриаксон, порошок, 2 г в Москве
Цефтриаксон, порошок, 2 г в Москве
- Бренд
- Ceftriaxone
- Действующее вещество
- Цефтриаксон
- Производитель
- Синтез
- Артикул
- 183688
- Дозировка
- 2г
- Количество в упаковке
- 1
- Рецептурный отпуск
- По рецепту
- Страна
- Россия
- Форма выпуска
- порошок
Инструкция по применению Цефтриаксон, порошок, 2 г
Способ применения
Стандартныйрежим дозирования
Внутривенно,внутримышечно.
Взрослыеи дети старше 12 лет ≥50 кг: по 1–2 г один разв сутки (каждые 24 часа). В тяжелых случаях или при инфекциях,возбудители которых обладают лишь умеренной чувствительностьюк цефтриаксону, суточную дозу можно увеличивать до 4 г.
Продолжительностьлечения зависит от течения заболевания. Как и всегда при антибиотикотерапии,введение препарата Цефтриаксон следует продолжать пациентам еще в течениеминимум 48–72 часов после нормализации температуры и подтвержденияэрадикации возбудителя.
Обычнокурс лечения составляет 4–14 дней; при осложненных инфекциях может потребоватьболее продолжительное введение.
Курслечения при инфекциях, вызванных Streptococcus pyogenes, долженсоставлять не менее 10 дней.
Введение
Общимправилом должно быть использование растворов сразу после приготовления.
Приготовленныерастворы сохраняют свою физическую и химическую стабильность в течение6 часов при комнатной температуре (или в течение 24 часов притемпературе 2–8 °С). В зависимости от концентрации ипродолжительности хранения цвет растворов может варьировать от бледно-желтогодо янтарного. Окраска раствора не влияет на эффективность илипереносимость препарата.
Длявнутримышечной инъекции 500 мг препарата Цефтриаксонрастворяют в 2 мл, а 1 г — в 3,5 мл 1% растворалидокаина и вводят глубоко в достаточно большую мышцу (ягодица). Рекомендуетсявводить не более 1 г в одну и ту же мышцу.
Раствор,содержащий лидокаин, нельзя вводить внутривенно.
Для внутривеннойинъекции 500 мг препарата Цефтриаксон растворяют в 5 мл, а1 г — в 10 мл стерильной воды для инъекций; вводят внутривенномедленно в течение 5 минут, предпочтительно в крупную вену.
Внутривеннаяинфузия должна длиться не менее 30 минут. Для приготовления раствораразводят 2 г препарата Цефтриаксон в 40 мл одного из следующихинфузионных растворов, не содержащих ионов кальция: 0,9% раствор натрияхлорида, 0,45% раствор натрия хлорида + 2,5% раствор декстрозы, 5% раствордекстрозы, 10% раствор декстрозы, 6% раствор декстрана в5% растворе декстрозы, 6–10% раствор гидроксиэтилкрахмала, вода дляинъекций. Растворы препарата Цефтриаксон нельзя смешивать или добавлятьв растворы, содержащие другие противомикробные препараты или другие растворители,за исключением перечисленных выше, из‑за возможной несовместимости.
Нельзяиспользовать для приготовления растворов препарата Цефтриаксон длявнутривенного введения и их последующего разведения растворители, содержащиекальций, такие как раствор Рингера или раствор Хартмана, из‑за возможногообразования преципитатов. Образование преципитатов кальциевых солейцефтриаксона может происходить и при смешивании препарата Цефтриаксон икальцийсодержащих растворов при использовании одного венозного доступа. Нельзяиспользовать цефтриаксон одновременно с кальцийсодержащими растворами длявнутривенного введения, в том числе с длительными инфузиями кальцийсодержащихрастворов, например, при парентеральном питании с использованием Y‑коннектора. Для всех групп пациентов, кроме новорожденных,возможно последовательное введение препарата Цефтриаксон и кальцийсодержащихрастворов при тщательном промывании инфузионных систем между вливаниямисовместимой жидкостью (см. раздел «Взаимодействие с другими лекарственнымисредствами»).
Непоступало сообщений о взаимодействии цефтриаксона и пероральныхкальцийсодержащих препаратов или взаимодействии цефтриаксона длявнутримышечного введения и кальцийсодержащих препаратов (для внутривенного илиперорального применения).
Дозированиев особых случаях
Пациентыс нарушением функции печени
Упациентов с нарушением функции печени нет необходимости уменьшать дозу приусловии отсутствия нарушений почек.
Пациентыс нарушением функции почек
Упациентов с нарушением функции почек нет необходимости уменьшать дозу приусловии отсутствия нарушений функции печени. Суточная доза препаратаЦефтриаксон не должна превышать 2 г лишь в случаях почечнойнедостаточности с клиренсом креатинина менее 10 мл/мин. Цефтриаксон невыводится при гемодиализе или перитонеальном диализе, поэтому введение пациентудополнительной дозы препарата Цефтриаксон после окончания диализа не требуется.
При сочетаниитяжелой почечной и печеночной недостаточности следует тщательно наблюдатьза эффективностью и безопасностью применения препарата.
Пациентыпожилого и старческого возраста
Обычныедозы для взрослых без поправок на возраст при условии отсутствия тяжелойпочечной и печеночной недостаточности.
Дети
Новорожденные,грудные дети и дети младше 12 лет
Приназначении препарата Цефтриаксон один раз в сутки рекомендуется придерживатьсяследующих режимов дозирования:
– новорожденные (до 14 дней): 20–50 мг/кг массы тела одинраз в сутки; суточная доза не должна превышать 50 мг/кг массы тела;
– новорожденные, грудные дети и дети младшего возраста (с15 дней до 12 лет): 20–80 мг/кг массы тела один раз в сутки;
– детям с массой тела свыше 50 кг назначают дозы для взрослых.
Недоношеннымдетям в возрасте до 41 недели включительно (суммарно гестационный ихронологический возраст) применение цефтриаксона противопоказано.
Цефтриаксонпротивопоказан новорожденным (≤28 дней), которым уже назначено илипредполагается внутривенное лечение кальцийсодержащими растворами, включаяпродолжительные кальцийсодержащие инфузии, например, при парентеральном питаниииз‑за риска образования преципитатов кальциевых солей цефтриаксона(см. раздел «Противопоказания»).
Груднымдетям и детям в возрасте до 12 лет внутривенные дозы в 50 мг/кг иливыше следует вводить капельно в течение не менее 30 минут. Новорожденнымвнутривенное введение следует проводить в течение 60 минут, чтобыснизить потенциальный риск развития билирубиновой энцефалопатии.
Менингит
При бактериальномменингите у грудных детей и детей младшего возраста лечение начинаютс дозы 100 мг/кг (но не более 4 г) 1 раз в сутки. Послеидентификации возбудителя и определения его чувствительности дозу можносоответственно уменьшить. Наилучшие результаты при менингококковом менингитедостигались при продолжительности лечения в 4 дня, при менингите, вызванномHaemophilus influenzae — 6 дней, Streptococcus pneumoniae —7 дней.
БолезньЛайма
50 мг/кг(высшая суточная доза — 2 г) взрослым и детям один раз в сутки втечение 14 дней.
Гонорея(вызванная пенициллиназообразующими и пенициллиназонеобразующими штаммами)
Однократноевнутримышечное введение 250 мг препарата Цефтриаксон взрослым пациентам идетям старше 12 лет ≥50 кг.
Острыйсредний отит
Прилечении острого среднего отита у детей рекомендуется однократное внутримышечноевведение в дозе 50 мг/кг (но не более 1 г).
Взрослымрекомендуется однократное внутримышечное введение в дозе 1–2 г. Согласноограниченным данным, в тяжелых случаях или при неэффективности предыдущейтерапии, препарат Цефтриаксон может быть эффективен при внутримышечном введениив дозе 1–2 г в сутки в течение 3 дней.
Профилактикапослеоперационных инфекций
Взависимости от степени инфекционного риска вводится 1–2 г препаратаЦефтриаксон однократно за 30–90 мин до начала операции. При операциях натолстой и прямой кишке хорошо зарекомендовало себя одновременное (нораздельное, см. раздел «Способ применения и дозы») введение препаратаЦефтриаксон и одного из 5‑нитроимидазолов, например, орнидазола.
Аналоги Ceftriaxone
Акции
Аптеки в Москве
- Время работы:
- Пн-Вс: 09:00-18:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 09:00-18:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 09:00-18:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 09:00-21:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 09:00-18:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Пт: 08:00-22:00; Сб-Вс: 09:00-21:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 09:00-21:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 09:00-21:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Время работы:
- Пн-Вс: 08:00-22:00
- Цена:
- 80.00₽
- Доставка:
- Завтра
- Способы оплаты:
- НаличныеОплата Картой
- Купить Цефтриаксон, порошок, 2 г в Москве – цена 80 руб. в аптеках «POLZAru».
- Официальная инструкция по применению Цефтриаксон, порошок, 2 г, сертификаты, отзывы и фото.