- Время работы:
- Пн-Вс: 08:00-22:00
- Цена:
- 401.00 ₽
- Доставка:
- Сегодня
- Способы оплаты:
- НаличныеОплата Картой
- Главная
- Лекарственные средства
- Сердечно-сосудистые заболевания
- Гипертензия, стенокардия
- Эксфорж
- Эксфорж, таблетки покрыт. плен. об. 10 мг+160 мг, 28 шт. в Москве
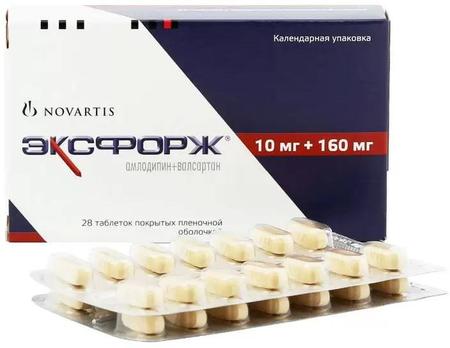

Эксфорж, таблетки покрыт. плен. об. 10 мг+160 мг, 28 шт. в Москве
- Бренд
- Эксфорж
- Действующее вещество
- ВалсартанАмлодипин
- Производитель
- Новартис Консьюмер Хелс
- Артикул
- 184071
- Дозировка
- 10 мг
- Количество в упаковке
- 28
- Рецептурный отпуск
- По рецепту
- Страна
- Испания
- Форма выпуска
- таблетки
Инструкция по применению Эксфорж, таблетки покрыт. плен. об. 10 мг+160 мг, 28 шт.
Способ применения
Препарат следует принимать внутрь, запивая небольшим количествомводы, 1 раз в сутки независимо от времени приема пищи.
Рекомендуемая суточная доза - 1 таблетка, содержащаяамлодипин+валсартан в дозе 5 мг+80 мг, или 5 мг+160 мг, или 10мг+160 мг (максимальная суточная доза по амлодипину).
Пациент, получающий валсартан и амлодипин в разныхтаблетках/капсулах, может быть переведен на прием препаратаЭксфорж® в таблетках, содержащих ту же дозировку действующихвеществ.
У пациентов, которым может потребоваться многокомпонентнаямедикаментозная терапия для достижения целевых значений АД, лечениеможет быть начато с препарата Эксфорж®. Следует тщательно оценитьотношение польза/риск при выборе препарата Эксфорж® в качественачальной терапии АГ.
Начинать прием препарата рекомендовано с дозы 5 мг+80 мг 1 раз всутки. Увеличивать дозу можно через 1-2 недели после началатерапии. Максимальная доза амлодипина и валсартана составляет 10мг+320 мг в сутки. Таблетки неделимые и не могут быть разделены наравные дозы.
Пациенты с нарушением функции почек
Для пациентов с нарушениями функции почек легкой и среднейстепени тяжести (СКФ ≥30 мл/мин/1,73 м2) коррекции начальной дозыне требуется.
Пациенты с нарушением функции печени
Вследствие наличия в составе валсартана и амлодипина препаратЭксфорж® следует с осторожностью применять у пациентов снарушениями функции печени и обструктивными заболеваниямижелчевыводящих путей. У пациентов данной категории следуетрассмотреть возможность применения начальной дозы препарата,содержащей наименьшую дозу амлодипина, т.е. одна таблетка,содержащая амлодипин+валсартан в дозе 5 мг+80 мг или 5 мг+160мг.
Применение у пациентов старше 65 лет
Поскольку оба компонента препарата одинаково хорошо переносятсяпри применении в соответствующих дозах у пожилых пациентов (ввозрасте 65 лет и старше) или у пациентов младше данной возрастнойкатегории, не требуется коррекции начальной дозы препарата у данныхпациентов. Следует рассмотреть возможность применения начальнойдозы препарата, содержащей наименьшую дозу амлодипина, т.е. однатаблетка, содержащая амлодипин+валсартан в дозе 5 мг+80 мг или 5мг+160 мг.
Применение у детей и подростков в возрасте до 18 лет
Поскольку данных о безопасности и эффективности препаратаЭксфорж® у детей и подростков (младше 18 лет) недостаточно,препарат не рекомендуется применять у пациентов даннойкатегории.
Противопоказания
Повышенная чувствительность к амлодипину, другим производным дигидропиридина, валсартану, а также другим вспомогательным компонентам препарата. Наследственный ангионевротический отек, ангионевротический отек на фоне предшествующей терапии антагонистами рецепторов ангиотензина II. Нарушение функции печени тяжелой степени (класс С по классификации Чайлд-Пью), билиарный цирроз, холестаз. Нарушение функции почек тяжелой степени (СКФ Беременность, планирование беременности и период грудного вскармливания. Тяжелая артериальная гипотензия (систолическое АД менее 90 мм рт.ст.), коллапс, кардиогенный шок. Обструкция выносящего тракта левого желудочка. Гемодинамически нестабильная сердечная недостаточность после острого инфаркта миокарда. Одновременное применение с алискиреном и препаратами, содержащими алискирен, у пациентов с сахарным диабетом и/или нарушением функции почек средней и тяжелой степени (СКФ
С осторожностью:
Гиперкалиемия, дефицит в организме натрия и/или уменьшение объема циркулирующей крови (ОЦК). Одновременное применение с калийсодержащими пищевыми добавками, калийсберегающими диуретиками, заменителями соли, а также другими препаратами, которые могут увеличивать содержание калия. Односторонний или двусторонний стеноз почечных артерий или стеноз артерии единственной почки. Митральный или аортальный стеноз и гипертрофическая обструктивная кардиомиопатия. Хроническая сердечная недостаточность III-IV функционального класса по классификации NYHA. Острый коронарный синдром, состояние после недавно перенесенного острого инфаркта миокарда. Нарушение функции печени легкой и средней степени по классификации Чайлд-Пью, обструктивные заболевания желчевыводящих путей.
- Одновременное применение с ингибиторами или индукторами изофермента CYP3A4.
Взаимодействия
Амлодипин
Симвастатин. Одновременное длительное применение симвастатина вдозе 80 мг/сут и амлодипина в дозе 10 мг/сут ведет к увеличениюэкспозиции симвастатина на 77%. Рекомендуется уменьшить дозусимвастатина у пациентов, принимающих амлодипин, до 20 мг/сут.
Ингибиторы изофермента CYP3A4. При применении амлодипина в дозе5 мг/сут одновременно с дилтиаземом в дозе 180 мг/сут у пожилыхпациентов отмечается замедление метаболизма амлодипина в 1,6 раз.При применении амлодипина одновременно с мощными ингибиторамиCYP3A4 (например, кетоконазол, итраконазол и ритонавир) возможновыраженное увеличение системной экспозиции амлодипина. Необходимо состорожностью применять амлодипин с ингибиторами изоферментаCYP3A4.
Грейпфрутовый сок. В связи с ингибированием изофермента CYP3A4при одновременном приеме с грейпфрутовым соком экспозицияамлодипина может увеличиваться. В клиническом исследовании у 20здоровых добровольцев, однако, не было выявлено значительныхизменений фармакокинетики при однократном приеме амлодипина в дозе10 мг с 240 мл грейпфрутового сока.
Индукторы изофермента CYP3A4 (противосудорожные средства(например, карбамазепин, фенобарбитал, фенитоин, фосфенитоин,примидон), рифампицин, растительные препараты, содержащие Зверобойпродырявленный). Нет данных о влиянии индукторов изофермента CYP3A4на амлодипин. Одновременное применение амлодипина с индукторамиизофермента CYP3A4 может приводить к уменьшению концентрацииамлодипина в плазме крови. Следует соблюдать осторожность приприменении амлодипина с препаратами индукторами изоферментаCYP3A4.
При монотерапии амлодипином не отмечено клинически значимоговзаимодействия с тиазидными диуретиками, β-адреноблокаторами,ингибиторами АПФ, нитратами длительного действия, нитроглицериномдля подъязычного применения, дигоксином, варфарином,аторвастатином, силденафилом, магния гидроксидом с гелем алюминиягидроксида и симетиконом, циметидином, нестероиднымипротивовоспалительными препаратами (НПВП), антибиотиками игипогликемическими лекарственными средствами для приема внутрь.
Этанол. Одновременный однократный и многократный приемамлодипина в дозе 10 мг с этанолом не влияет на фармакокинетикупоследнего.
Валсартан
Двойная блокада РААС при применении антагонистов рецепторовангиотензина II, ингибиторов АПФ или алискирена
Одновременное применение АРА II, в том числе валсартана, сдругими препаратами, влияющими на РААС, приводит к увеличениючастоты возникновения случаев артериальной гипотензии,гиперкалиемии, нарушения функции почек. Двойная блокада РААСпосредством одновременного применения ингибитора АПФ, АРА II илиалискирена не рекомендована в общей популяции. Однако, в томслучае, если комбинированная терапия указанными препаратамиявляется абсолютно необходимой, такое применение должноосуществляться под тщательным наблюдением врача, с частым контролемпоказателей АД, функции почек, а также содержания электролитовплазмы крови. Не следует проводить одновременную терапиюингибиторами АПФ и АРА II у пациентов с диабетическойнефропатией.
Одновременное применение препаратов, содержащих АРА II, включаяпрепарат Эксфорж®, с другими средствами, влияющими на РААС, в томчисле с алискиреном, противопоказано у пациентов с сахарнымдиабетом и/или нарушением функции почек средней или тяжелой степени(СКФ
Препараты и вещества, влияющие на содержание калия в сывороткекрови. При одновременном применении с биологически активнымидобавками, содержащими калий, калийсберегающими диуретиками,эплереноном, калийсодержащими заменителями соли или с другимипрепаратами, которые могут вызывать увеличение содержания калия вкрови (например, с гепарином и др.), следует соблюдать осторожностьи проводить регулярный контроль содержания калия в крови.
НПВП, включая селективные ингибиторы циклооксигеназы-2 (ЦОГ-2).Применение антагонистов рецепторов ангиотензина II одновременно сНПВП, включая ингибиторы ЦОГ-2, может привести к ослаблениюантигипертензивного действия. У пожилых пациентов, пациентов сосниженным ОЦК (в том числе получающих терапию диуретическимисредствами) или с нарушением функции почек одновременное применениеАРА II и НПВП, включая ингибиторы ЦОГ-2, может увеличить рискразвития нарушений функции почек. В начале терапии или прикоррекции режима дозирования у пациентов, принимающих АРА II иНПВП, включая ингибиторы ЦОГ-2, рекомендуется проводить контрольфункции почек.
Препараты лития. При одновременном применении препаратов лития сингибиторами АПФ и АРА II отмечалось обратимое увеличениесодержания лития в сыворотке крови и усиление токсическихпроявлений, в связи с чем при одновременном применении указанныхпрепаратов рекомендовано проводить контроль содержания лития всыворотке крови. При одновременном применении диуретиков спрепаратами лития риск развития его токсического эффекта можетдополнительно увеличиваться при добавлении препарата Эксфорж® ктерапии.
Белки-переносчики. По данным in vitro исследования ткани печеничеловека валсартан является субстратом белка-переносчика ОАТР1В1 иMRP2. Одновременное применение валсартана с ингибиторамибелка-переносчика ОАТР1В1 (рифампицин, циклоспорин) и с ингибиторомбелка-переносчика MRP2 (ритонавир) может приводить к увеличениюсистемной биодоступности валсартана.
Установлено, что при монотерапии валсартаном отсутствуетклинически значимое взаимодействие со следующими лекарственнымисредствами: циметидин, варфарин, фуросемид, дигоксин, атенолол,индометацин, гидрохлоротиазид, амлодипин, глибенкламид.
Побочные действия
Безопасность применения препарата Эксфорж® оценена более чем у 2600 пациентов.
Критерии оценки частоты нежелательных реакций: очень часто (>10% случаев); часто (1–10%); иногда (0,1–1%); редко (0,001–0,1%); в отдельных случаях (<0,001%). В пределах каждой группы, выделенной по частоте встречаемости, побочные реакции распределены в порядке уменьшения их важности.
Со стороны дыхательной системы: часто — назофарингит, грипп.
Аллергические и иммунологические реакции: редко — повышенная чувствительность.
Со стороны органов чувств: редко — нарушения зрения, шум в ушах; иногда — головокружение, связанное с нарушением функции вестибулярного аппарата.
Психические нарушения: редко — тревожность.
Со стороны ЦНС и периферической нервной системы: часто — головная боль; иногда — головокружение, сонливость, ортостатическое головокружение, парестезии.
Со стороны дыхательной системы: иногда — кашель, боль в глотке и гортани.
Со стороны сердечно-сосудистой системы: иногда — тахикардия, сердцебиение, ортостатическая гипотензия; редко — синкопальное состояние, выраженное снижение АД.
Со стороны пищеварительной системы: иногда — диарея, тошнота, боль в животе, запор, сухость во рту.
Дерматологические реакции: иногда — кожная сыпь, эритема; редко — гипергидроз, экзантема, зуд.
Со стороны костно-мышечной системы: иногда — отечность суставов, боль в спине, артралгии; редко — мышечные спазмы, чувство тяжести во всем теле.
Со стороны мочеполовой системы: редко — поллакиурия, полиурия, эректильная дисфункция.
Прочие: часто — пастозность, отек лица, периферические отеки, повышенная утомляемость, приливы крови к лицу, астения, чувство жара.
В сравнительных и плацебо-контролируемых клинических исследованиях частота периферических отеков была достоверно ниже у пациентов, получавших комбинацию амлодипина с валсартаном (5,8%), чем у пациентов, получавших монотерапию амлодипином (9%).
Лабораторные показатели: повышение азота мочевины крови (более 3,1 ммоль/л) наблюдалось незначительно чаще в группах, получавших амлодипин/валсартан (5,5%) и валсартан в виде монотерапии (5,5%), по сравнению с группой, получавшей плацебо (4,5%).
Нежелательные явления, о которых сообщалось ранее при применении каждого из компонентов, могут иметь место при применении Эксфоржа, даже если они не наблюдались в клинических исследованиях.
Амлодипин
В тех клинических исследованиях, где амлодипин применяли в качестве монотерапии, отмечались также другие нежелательные явления (независимо от их причинной связи с изучаемым препаратом): наиболее часто — тошнота; реже — алопеция, изменение частоты дефекации, диспепсия, одышка, ринит, гастрит, гиперплазия десен, гинекомастия, гипергликемия, эректильная дисфункция, учащение мочеиспускания, лейкопения, общее недомогание, лабильность настроения, сухость во рту, миалгия, периферическая невропатия, панкреатит, гепатит, повышенное потоотделение, тромбоцитопения, васкулит, ангионевротический отек, многоформная эритема.
В продолжительном плацебо-контролируемом исследовании (PRAISE-2) у больных с сердечной недостаточностью III и IV степени по классификации NYHA неишемической этиологии при применении амлодипина отмечалось увеличение частоты возникновения отека легких при отсутствии значимых различий по частоте развития ухудшения течения сердечной недостаточности в сравнении с плацебо.
В редких случаях в начале терапии блокаторами медленных кальциевых каналов или при повышении дозы блокаторов медленных кальциевых каналов, особенно у пациентов страдающих тяжелой формой ИБС, отмечалось повышение частоты, длительности и выраженности стенокардии или развитие острого инфаркта миокарда. Также на фоне терапии БМКК наблюдались случаи развития аритмии (включая желудочковую тахикардию и фибрилляцию предсердий). Не представляется возможным отличить возникновение данных нежелательных явлений от естественного течения основного заболевания.
Валсартан
В клинических исследованиях при применении валсартана в качестве монотерапии были отмечены следующие нежелательные явления (независимо от их причинной связи с изучаемым препаратом): вирусные инфекции, инфекции верхних дыхательных путей, синусит, ринит, нейтропения, бессонница.
Нейтропения была выявлена у 1,9% больных, получавших валсартан, и 1,6% больных, получавших ингибитор АПФ.
В контролируемых клинических исследованиях у 3,9 и 16,6% больных с сердечной недостаточностью, получавших валсартан, было отмечено повышение уровня креатинина и азота мочевины крови более чем на 50% соответственно. Для сравнения — у больных, получавших плацебо, повышение креатинина и азота мочевины наблюдалось в 0,9 и 6,3% случаев.
Удвоение содержания сывороточного креатинина было выявлено у 4,2% пациентов после перенесенного инфаркта миокарда, получавших валсартан и у 3,4% получавших каптоприл.
В контролируемых клинических исследованиях у 10% пациентов с сердечной недостаточностью было отмечено повышение концентрации калия сыворотки более чем на 20%. Для сравнения, у больных, получавших плацебо, повышение концентрации калия наблюдалось в 5,1% случаев.
Передозировки
Данные о случаях передозировки препарата в настоящее время отсутствуют.
Симптомы: при передозировке валсартана можно ожидать развитие выраженного снижения АД и головокружения. Передозировка амлодипина может привести к чрезмерной периферической вазодилатации и возможной рефлекторной тахикардии. Сообщалось также о возникновении выраженной и длительной системной артериальной гипотензии вплоть до развития шока с летальным исходом.
Лечение: при случайной передозировке следует вызвать рвоту (если препарат был принят недавно) или провести промывание желудка. Применение активированного угля у здоровых добровольцев сразу или через 2 ч после приема амлодипина значительно уменьшало его абсорбцию.
При клинически выраженной артериальной гипотензии, вызванной препаратом Эксфорж®, следует уложить больного с приподнятыми ногами, принять активные меры по поддержанию деятельности сердечно-сосудистой системы, включая частый контроль функции сердца и дыхательной системы, ОЦК и количества выделяемой мочи. При отсутствии противопоказаний с целью восстановления сосудистого тонуса и АД возможно применение (с осторожностью) вазоконстриктора. В/в введение кальция глюконата может быть эффективным для устранения блокады кальциевых каналов. Выведение валсартана и амлодипина при проведении гемодиализа маловероятно.
Состав
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
|---|---|
| активные вещества: | |
| амлодипина бесилат | 6,94/6,94/13,87 мг |
| (что соответствует 5/5/10 мг амлодипина соответственно) | |
| валсартан | 80/160/160 мг |
| вспомогательные вещества: МКЦ — 54,06/109,06/ 108,13 мг; кросповидон — 20/40/40 мг, магния стеарат — 4,5/9/9 мг, кремния диоксид коллоидный — 1,5/3/3 мг | |
| пленочная оболочка: Premix белая (гипромеллоза, титана диоксид, полиэтиленгликоль 4000, тальк) — 4,4/ 7,15/ 11,93 мг; Premix желтая (гипромеллоза, железа оксид желтый, полиэтиленгликоль 4000, тальк) — 3,6/ 5,85/ 1,04 мг; Premix красная (гипромеллоза, железа оксид красный, полиэтиленгликоль, тальк) (содержится в таблетках дозировкой 10 мг/160 мг) — 0,03 мг; вода очищенная — достаточное количество |
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
|---|---|
| активные вещества: | |
| амлодипина безилат | 6,94/13,87 мг |
| (что эквивалентно 5 мг или 10 мг амлодипина основания, соответственно) | |
| валсартан | 320 мг |
| вспомогательные вещества: МКЦ — 501,96/ 495,03 мг, кросповидон — 60 мг, магния стеарат — 18,9 мг, карбоксиметилкрахмал натрия — 6 мг, кремния диоксид коллоидный — 6 мг, краситель железа оксид желтый (Е172) — 0,2 мг | |
| оболочка Premix для дозировки 5+320 мг: Premix желтая — 23,75 мг (гипромеллоза — 71,43%, краситель железа оксид желтый (Е172) — 14,29%, макрогол 4000 — 7,14%, тальк — 7,14%), Premix красная — 1,25 мг (гипромеллоза — 71,43%, краситель железа оксид красный (Е172) — 14,29%, макрогол 4000 — 7,14%, тальк — 7,14%) | |
| оболочка Premix для дозировки 10+320 мг: Premix белая — 13,75 мг (гипромеллоза — 71,43%, титана диоксид — 14,29%, макрогол 4000 — 7,14%, тальк — 7,14%), Premix желтая 11,25 мг (гипромеллоза — 71,43%, краситель железа оксид желтый (Е172) — 14,29%, макрогол 4000 — 7,14%, тальк — 7,14%) |
.
Описание лекарственной формы
Таблетки, покрытые пленочной оболочкой, 5/80 мг: темно-желтого цвета, круглые со скошенными краями, с надпечаткой «NVR» на одной стороне и «NV» — на другой.
Таблетки, покрытые пленочной оболочкой, 5/160 мг: темно-желтого цвета, овальные со скошенными краями, с надпечаткой «NVR» на одной стороне и «ECE» — на другой.
Таблетки, покрытые пленочной оболочкой, 10/160 мг: светло-желтого цвета, овальные со скошенными краями, с надпечаткой «NVR» на одной стороне и «UIC» — на другой.
Фармакокинетика
Фармакокинетика валсартана и амлодипина характеризуется линейностью.
Амлодипин
Всасывание. После приема внутрь амлодипина в терапевтических дозах Cmax амлодипина в плазме крови достигается через 6–12 ч. Величина абсолютной биодоступности составляет в среднем 64–80%. Прием пищи не влияет на биодоступность амлодипина.
Распределение. Кажущийся VSS составляет приблизительно 21 л/кг. В исследованиях с амлодипином in vitro показано, что у пациентов с артериальной гипертензией приблизительно 97,5% циркулирующего препарата связывается с белками плазмы крови.
Метаболизм. Амлодипин интенсивно (приблизительно 90%) метаболизируется в печени с образованием активных метаболитов.
Выведение. Выведение амлодипина из плазмы носит двухфазный характер с T1/2 приблизительно от 30 до 50 ч. Равновесная концентрация в плазме крови достигается после применения в течение 7–8 дней. 10% неизмененного амлодипина и 60% амлодипина в виде метаболитов выводится почками.
Валсартан
Всасывание. После приема внутрь валсартана Cmax в плазме крови достигается через 2–3 ч. Средняя абсолютная биодоступность — 23%. Фармакокинетическая кривая валсартана имеет нисходящий мультиэкспоненциальный характер (T1/2α <1 ч и T1/2β — около 9 ч). При приеме валсартана с пищей отмечается снижение биодоступности (по значению AUC) на 40% и Cmax в плазме крови почти на 50%, хотя приблизительно через 8 ч после приема препарата концентрации валсартана в плазме крови в группе пациентов, принимавших его с пищей, и в группе, принимавшей натощак, выравниваются. Уменьшение AUC, однако, не сопровождается клинически значимым снижением терапевтического эффекта, поэтому валсартан можно назначать вне зависимости от времени приема пищи.
Распределение. VSS валсартана в равновесном состоянии после в/в введения составлял около 17 л, что указывает на отсутствие экстенсивного распределения валсартана в тканях. Валсартан в значительной степени связывается с белками сыворотки крови (94–97%), преимущественно с альбуминами.
Метаболизм. Валсартан не подвергается выраженному метаболизму (около 20% принятой дозы определяется в виде метаболитов). Гидроксильный метаболит определяется в плазме крови в низких концентрациях (менее чем 10% от AUC валсартана). Этот метаболит фармакологически активен.
Выведение. Валсартан выводится в основном в неизмененном виде через кишечник (около 83% дозы) и почками (около 13% дозы). После в/в введения, плазменный Cl валсартана составляет около 2 л/ч, почечный Cl — 0,62 л/ч (около 30% общего клиренса). T1/2 валсартана — 6 ч.
Амлодипин/Валсартан
После приема внутрь препарата Эксфорж® Cmax валсартана и амлодипина достигаются через 3 и 6–8 ч соответственно. Скорость и степень абсорбции препарата эквивалентны биодоступности валсартана и амлодипина при приеме каждого из них в виде отдельных таблеток.
Фармакокинетика в особых клинических случаях
Фармакокинетические особенности применения препарата Эксфорж® у детей до 18 лет не установлены.
Пациенты пожилого возраста.Время достижения Cmax амлодипина в плазме крови у молодых и пожилых пациентов одинаково. У пациентов пожилого возраста клиренс амлодипина незначительно снижен, что приводит к увеличению AUC и T1/2.
У пожилых пациентов системное воздействие валсартана было несколько более выраженным, чем у молодых, однако эти показатели не были клинически значимыми. Поскольку переносимость компонентов препарата у пожилых и у более молодых больных одинаково хорошая, рекомендуется применять обычные режимы дозирования.
Пациенты с нарушением функции почек.У пациентов с нарушением функции почек фармакокинетические параметры амлодипина существенно не изменяются. Не было выявлено корреляции между функцией почек (клиренс) и системным воздействием валсартана (AUC) у пациентов с различной степенью нарушения функции почек. Не требуется изменение начальной дозы у пациентов с начальными и умеренными нарушениями функции почек (Cl креатинина — 30–50 мл/мин).
Пациенты с нарушением печени.Пациенты с печеночной недостаточностью имеют сниженный клиренс амлодипина, что приводит к повышению AUC приблизительно на 40–60%. В среднем, у пациентов с хроническими заболеваниями печени слабой и умеренной степени биодоступность (AUC) валсартана удваивается по сравнению со здоровыми добровольцами (соответствующего возраста, пола и массы тела).
Фармакодинамика
Препарат Эксфорж® является комбинацией 2 антигипертензивных препаратов с дополняющим друга механизмом контроля АД: амлодипин, производное дигидропиридина, относится к классу блокаторов «медленных» кальциевых каналов (БМКК), валсартан — к классу антагонистов рецепторов ангиотензина II. Комбинация этих компонентов обладает взаимно дополняющим гипотензивным действием, что приводит к более выраженному снижению АД по сравнению с таковым на фоне монотерапии каждым препаратом.
Амлодипин
Амлодипин, входящий в состав препарата Эксфорж®, ингибирует трансмембранное поступление ионов кальция в кардиомиоциты и гладкомышечные клетки сосудов. Механизм антигипертензивного действия амлодипина связан с прямым расслабляющим эффектом на гладкие мышцы сосудов, вызывающим уменьшение ОПСС и снижение АД.
После приема в терапевтических дозах у пациентов с артериальной гипертензией амлодипин вызывает расширение сосудов, приводящее к снижению АД (в положении больного «лежа» и «стоя»). Снижение АД не сопровождается существенным изменением ЧСС и уровня катехоламинов при длительном применении.
Концентрации препарата в плазме крови коррелируют с клиническим эффектом как у молодых, так и у пожилых пациентов.
При артериальной гипертензии у пациентов с нормальной функцией почек амлодипин в терапевтических дозах приводит к уменьшению сопротивления почечных сосудов, повышению скорости клубочковой фильтрации и эффективного почечного кровотока без изменения фильтрационной фракции и уровня протеинурии.
Также как и при применении других БМКК, прием амлодипина у пациентов с нормальной функцией левого желудочка (ЛЖ) вызывал изменение гемодинамических показателей функции сердца в покое и при физической нагрузке: отмечалось небольшое повышение сердечного индекса без значительного влияния на максимальную скорость нарастания давления в ЛЖ (dP/dt), конечного дАД и объема ЛЖ. Гемодинамические исследования у интактных животных и людей показали, что снижение АД под влиянием амлодипина в диапазоне терапевтических доз не сопровождается отрицательным инотропным действием даже при одновременном применении с бета-адреноблокаторами.
Амлодипин не изменяет функцию синоатриального узла или AV проводимость у интактных животных и человека. При применении амлодипина в комбинации с бета-адреноблокаторами у пациентов с артериальной гипертензией или стенокардией снижение АД не сопровождается нежелательными изменениями параметров ЭКГ.
Доказана клиническая эффективность амлодипина у пациентов с хронической стабильной стенокардией, вазоспастической стенокардией и ангиографически подтвержденным поражением коронарных артерий.
Валсартан
Валсартан — активный и специфический антагонист рецепторов ангиотензина II, предназначенный для приема внутрь. Он действует избирательно на рецепторы подтипа AT1, которые ответственны за известные эффекты ангиотензина II. Увеличение плазменной концентрации свободного ангиотензина II вследствие блокады AT1-рецепторов под влиянием валсартана может стимулировать незаблокированные АТ2-рецепторы, которые противодействуют эффектам блокады AT1-рецепторов. Валсартан не имеет сколько-нибудь выраженной агонистической активности в отношении AT1-рецепторов. Сродство валсартана к рецепторам подтипа AT1 примерно в 20000 раз выше, чем к рецепторам подтипа АТ2.
Валсартан не ингибирует АПФ, также известный как кининаза II, который превращает ангиотензин I в ангиотензин II и вызывает разрушение брадикинина.
При применении антагонистов ангиотензина II не происходит ингибирование АПФ и накопление брадикинина или субстанции Р, поэтому развитие сухого кашля маловероятно.
В сравнительных клинических исследованиях валсартана с ингибитором АПФ частота развития сухого кашля была достоверно ниже (p<0,05) у больных, получавших валсартан (у 2,6% пациентов, получавших валсартан, и у 7,9% — получавших ингибитор АПФ). В клиническом исследовании, включавшем больных, у которых ранее при лечении ингибитором АПФ развивался сухой кашель, при лечении валсартаном это осложнение было отмечено в 19,5% случаев, при лечении тиазидным диуретиком — в 19% случаев. В то же время, в группе больных, получавших лечение ингибитором АПФ, кашель наблюдался в 68,5% случаев (p<0,05). Валсартан не вступает во взаимодействие и не блокирует рецепторы гормонов или ионные каналы, имеющие важное значение для регуляции функций сердечно-сосудистой системы.
При лечении валсартаном больных с артериальной гипертензией отмечается снижение АД, не сопровождающееся изменением ЧСС.
Антигипертензивный эффект проявляется в течение 2 ч у большинства больных после разового приема препарата. Максимальное снижение АД развивается через 4–6 ч. После приема препарата гипотензивны эффект сохраняется более 24 ч. При повторном применении максимальное снижение АД вне зависимости от принятой дозы обычно достигается в пределах 2–4 нед и поддерживается на достигнутом уровне в ходе длительной терапии. Резкое прекращение приема валсартана не сопровождается резким повышением АД или другими нежелательными клиническими последствиями. Применение валсартана у пациентов с хронической сердечной недостаточностью (II–IV класса по классификации NYHA) приводит к значительному уменьшению числа госпитализаций. Этот эффект максимально выражен у больных, не получающих ингибиторы АПФ или бета-адреноблокаторы. При приеме валсартана у пациентов с левожелудочковой недостаточностью (стабильное клиническое течение) или с нарушением функции ЛЖ после перенесенного инфаркта миокарда отмечается снижение сердечно-сосудистой смертности.
Амлодипин/Валсартан
У пациентов с артериальной гипертензией, получавших препарат Эксфорж® 1 раз/сут антигипертензивный эффект сохранялся в течение 24 ч.
Препарат Эксфорж® в дозах 5/80 и 5/160 мг у больных с исходным сАД 153–157 мм рт.ст. и дАД ≥95 и <110 мм рт.ст., снижает АД на 20–28/14–19 мм рт.ст. (по сравнению с 7–13/7–9 мм рт.ст. при приеме плацебо).
Препарат Эксфорж® в дозе 10/160 и 5/160 мг нормализует АД (снижение дАД в положении «сидя» <90 мм рт.ст.) у 75 и 62% больных с неадекватным контролем АД на фоне монотерапии валсартаном в дозе 160 мг/сут .
Препарат Эксфорж® в дозе 10/160 мг нормализует АД у 78% больных с неадекватным контролем АД на фоне монотерапии амлодипином в дозе 10 мг.
У больных с артериальной гипертензией при комбинации валсартана в дозе 160 мг с амлодипином в дозах 10 и 5 мг достигается дополнительное снижение сАД и дАД на 6,0/4,8 мм рт.ст. и 3,9/2,9 мм рт.ст. соответственно по сравнению с пациентами, которые продолжали получать только валсартан в дозе 160 мг или только амлодипин в дозе 5 и 10 мг.
При титровании дозы препарата Эксфорж® от 5/160 до 10/160 мг у больных с артериальной гипертензией с дАД ≥110 и <120 мм рт.ст. наблюдается снижение АД в положении «сидя» на 36/29 мм рт.ст., сопоставимое со снижением АД при титровании дозы комбинации ингибитора АПФ и тиазидного диуретика.
В двух долгосрочных исследованиях с длительным периодом наблюдения эффект препарата Эксфорж® сохранялся в течение 1 года. Внезапное прекращение приема препарата Эксфорж® не сопровождается резким повышением АД.
У пациентов с достигнутым адекватным контролем АД, но развившимися выраженными отеками на фоне монотерапии амлодипином при применении комбинированной терапии достигался сопоставимый контроль АД при меньшей вероятности развития отеков.
Терапевтическая эффективность препарата Эксфорж® не зависит от возраста, пола и расы пациента.
Показания
Артериальная гипертензия (для пациентов, которым показана комбинированная терапия).
При беременности
Беременность
Как и для любого другого препарата, оказывающего прямое действиена РААС, применение препарата Эксфорж® противопоказано прибеременности. Безопасность применения амлодипина у беременныхженщин не установлена. В доклинических исследованияхпродемонстрирована репродуктивная токсичность при применениивысоких доз амлодипина у животных. Учитывая механизм действия АРАII, нельзя исключить риск для плода при применении препаратаЭксфорж® в I триместре беременности. При планировании беременностирекомендуется перевести пациентку на альтернативную гипотензивнуютерапию с учетом профиля безопасности, за исключением случаев,когда лечение АРА II считается необходимым. В случае, еслибеременность диагностирована в период лечения препаратом Эксфорж®,препарат следует отменить как можно раньше и, при необходимости,начать альтернативное лечение.
Известно, что применение АРА II во II и III триместребеременности вызывает развитие фетотоксических эффектов (нарушениефункции почек, маловодие, замедление окостенения костей черепаплода) и неонатальные токсические эффекты (почечнаянедостаточность, артериальная гипотензия, гиперкалиемия).
При приеме блокаторов рецепторов ангиотензина II во II триместребеременности рекомендуется проведение ультразвукового обследованияфункции почек и состояния костей черепа плода. Новорожденных,матери которых получали терапию АРА II, следует тщательно наблюдатьотносительно развития артериальной гипотензии.
Грудное вскармливание
Неизвестно, выделяется ли валсартан с грудным молоком. Отмеченовыделение амлодипина с грудным молоком. Подсчитано, что младенецполучает в пределах 3-7%, максимально 15% от материнской дозы.Влияние амлодипина на младенцев не изучено. Применение препарата вовремя грудного вскармливания противопоказано.
Фертильность
Клинические исследования влияния препарата Эксфорж® нафертильность отсутствуют.
Данных о влиянии валсартана на фертильность у человека нет.Клинических данных, касающихся потенциального влияния амлодипина нафертильность, недостаточно. У некоторых пациентов, находящихся налечении блокаторами кальциевых каналов, наблюдались обратимыебиохимические изменения в головке сперматозоидов.
Специальные инструкции
Дефицит натрия и/или уменьшение ОЦК
В плацебо-контролируемых исследованиях при применении препаратау пациентов с неосложненной АГ в 0,4% случаев наблюдаласьвыраженная артериальная гипотензия. У пациентов с активированнойРААС (например, при дефиците ОЦК и/или натрия у пациентов,получающих высокие дозы диуретиков), при приеме АРА II, возможноразвитие симптоматической артериальной гипотензии. Перед началомлечения препаратом Эксфорж® следует провести коррекцию содержаниянатрия и/или ОЦК или начинать терапию под тщательным медицинскимнаблюдением.
В случае возникновения выраженного снижения АД пациента следуетуложить с приподнятым ножным концом, при необходимости провести в/винфузию 0,9% раствора натрия хлорида. После стабилизации АД лечениепрепаратом Эксфорж® может быть продолжено.
Гиперкалиемия
При одновременном применении препарата с биологически активнымидобавками, содержащими калий, калийсберегающими диуретиками,калийсодержащими заменителями соли или с другими препаратами,которые могут вызывать повышение содержания калия в крови(например, с гепарином), следует соблюдать осторожность и проводитьрегулярный контроль содержания калия в крови.
Стеноз почечной артерии
У пациентов с односторонним или двусторонним стенозом почечнойартерии или стенозом артерии единственной почки прием препаратаЭксфорж® может сопровождаться повышением концентраций мочевины икреатинина в сыворотке крови, в связи с чем препарат следует состорожностью применять у данной категории пациентов.
Нарушения функции почек
Не требуется коррекции дозы препарата у пациентов с нарушениемфункции почек легкой и средней степени.
Одновременное применение АРА II, в том числе валсартана, илиингибиторов АПФ с алискиреном и препаратами, содержащими алискирен,противопоказано у пациентов с сахарным диабетом и/или нарушениямифункции почек средней и тяжелой степени (СКФ
Нет данных по применению препарата у пациентов странсплантированной почкой.
Нарушения функции печени
Валсартан выводится главным образом в неизмененном виде черезкишечник с желчью, в то время как амлодипин интенсивнометаболизируется в печени. Следует соблюдать осторожность приприменении препарата Эксфорж® у пациентов с заболеваниями печени(особенно при обструктивных заболеваниях желчевыводящих путей),сопровождающихся нарушениями функции печени.
Ангионевротический отек
При применении валсартана отмечено развитие ангионевротическогоотека, в том числе отека гортани и голосовых связок, приводящее кобструкции дыхательных путей, и/или отека лица, губ, глотки и/илиязыка; у некоторых из таких пациентов отмечено развитиеангионевротического отека в анамнезе при применении другихлекарственных препаратов, в том числе ингибиторов АПФ. В случаеразвития ангионевротического отека терапию препаратом следуетнезамедлительно прекратить без повторного возобновления.
Сердечная недостаточность, состояние после перенесенногоинфаркта миокарда
В целом, у пациентов с хронической сердечной недостаточностьюIII-IV функционального класса по классификации NYHA следует состорожностью применять блокаторы "медленных" кальциевыхканалов.
Применение ингибиторов АПФ или АРА II в случаях, когда состояниефункции почек зависит от активности РААС (например, у пациентов ссердечной недостаточностью) ассоциировалось с развитием олигуриии/или прогрессирующей азотемии, в редких случаях приводило к остройпочечной недостаточности и/или летальному исходу. При оценкесостояния пациента с острой сердечно-сосудистой недостаточностью вовсех случаях следует определять состояние функции почек.
Острый инфаркт миокарда
В начале терапии амлодипином (или при увеличении его дозы)возможно усугубление стенокардии и развитие острого инфарктамиокарда, в особенности у пациентов с тяжелой ишемической болезньюсердца.
Влияние на способность к вождению автотранспорта и управлениюмеханизмами
Отсутствуют данные о влиянии препарата на способность управлятьтранспортными средствами и осуществлять работу с механизмами. Всвязи с возможным возникновением головокружения или повышеннойутомляемости следует соблюдать осторожность при осуществленииуказанных видов деятельности.
Фармакологическое действие
Гипотензивное средство комбинированное (БМКК+ангиотензина IIрецепторов антагонист).
Условия хранения
t не выше 25 °C, в ориг. уп.
Аналоги Эксфорж
Акции
Аптеки в Москве
Цены на Эксфорж в других городах
- Купить Эксфорж, таблетки покрыт. плен. об. 10 мг+160 мг, 28 шт. в Москве можно в удобной для вас аптеке
- Цена на Эксфорж, таблетки покрыт. плен. об. 10 мг+160 мг, 28 шт. - 401 руб.
- Инструкция по применению для Эксфорж, таблетки покрыт. плен. об. 10 мг+160 мг, 28 шт.